Obwohl ich in Spanien aufgewachsen bin und dort auch meine wissenschaftliche Karriere begonnen habe, bevor das erste Humangenom überhaupt sequenziert war, kam es mir nie in den Sinn, dass Forschung extrem eurozentrisch ist (also nur auf Populationen europäischer Abstammung fokussiert). Auch als ich 2004 nach Florida zog, einem Staat mit einem hohen lateinamerikanischen Bevölkerungsanteil, und dennoch ausschließlich mit Proben von Teilnehmer*innen überwiegend europäischer Abstammung arbeitete, stellte ich den Grund dahinter nie Frage.
2006 jedoch reiste ich ins Land der Inkas, nach Peru, wo ich einen Vortrag bei einer Konferenz der lateinamerikanischen Gesellschaft für Bewegungsstörungen halten sollte. Und diese Reise öffnete mir die Augen dafür, dass Lateinamerikaner*innen im Forschungsfeld unterrepräsentiert sind. Spezialist*innen für Bewegungsstörungen aus fast allen lateinamerikanischen Ländern lauschten meinem Vortrag über die Genetik der Parkinsonkrankheit und dieses neue Gen mit Namen LRRK2, das bei 1 bis 2 % der Patient*innen Parkinson auszulösen schien. Während der Frage- & Antwortrunde fragten mich zahlreiche Kliniker*innen, ob ich wüsste, wie häufig es Mutationen bei diesem Gen bei Lateinamerikaner*innen gäbe und wie sie alle ihre Patient*innen testen lassen könnten. Und da, vor diesem Publikum, musste ich zugeben, dass dies in unserem Forschungsfeld nicht bekannt war. Alle Studien waren an Personen europäischer Abstammung durchgeführt worden.
Obwohl Lateinamerikaner*innen einen Anteil europäischer Abstammung aufweisen, variiert dieser je nach Person sehr stark, sogar innerhalb desselben Landes. Tatsächlich ergaben Studien an Patienten eben dieser Mediziner vor einigen Jahren, dass die Häufigkeit von Mutationen in LRRK2 stark mit dem durchschnittlichen Anteil europäischer Vorfahren in den einzelnen Ländern zusammenhängt. In Ländern wie Peru, wo am wenigsten europäisches genetisches Material vorhanden ist, ist die Mutationshäufigkeit am niedrigsten.
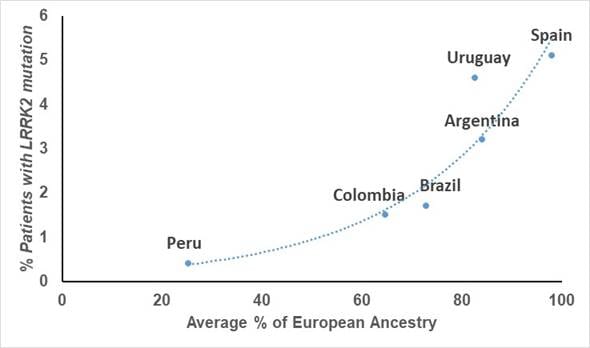
Diagramm zur Beziehung zwischen der Häufigkeit von LRRK2-Mutationen und dem Anteil der europäischen Abstammung in jedem Land (aus Zabetian et al. 2017)
Studien an einem anderen Parkinson-Gen – GBA – haben gezeigt, dass nicht nur die Häufigkeit, sondern auch die Art der Mutation, die man in einem lateinamerikanischen Land findet, unterschiedlich und manchmal auch populationsspezifisch sind.
All diese Erkenntnisse haben wichtige Auswirkungen, wenn man etwa entscheiden soll, auf welche Gene in einer bestimmten Population getestet werden soll oder welche therapeutischen Ziele in den einzelnen Patientenkohorten am wichtigsten wären. Mit zunehmendem Wissen über die Rolle der Genetik bei Morbus Parkinson werden diese Informationen entscheidend sein für die Vorhersage, wer ein hohes Risiko hat, diese (oder eine beliebige andere) Krankheit zu entwickeln. Dies gilt gleichermaßen für die vielen verschiedenen Ergebnisse, die durch die Genetik beeinflusst werden können.
Und obwohl ich hier über Lateinamerikaner*innen gesprochen habe, gilt dies ebenso für viele andere große unterrepräsentierte Bevölkerungsgruppen, etwa aus Afrika, Indien oder Südostasien. Dies ist ein enormes Problem, das wir lösen müssen – zumal wir auf Präzisionsmedizin bzw. personalisierte Medizin hinarbeiten, denn dieser Mangel an Wissen wird die bereits bestehenden gesundheitlichen Ungleichheiten noch vergrößern.
Die gute Nachricht lautet, dass nun größeres Bewusstsein für dieses Thema besteht, was weltweite Anstrengungen zur Behebung dieses Problems angefacht hat. Das Global Parkinson’s Genetic Program (GP2) von Aligning Science Across Parkinson’s (ASAP) bringt Forscher*innen aus der ganzen Welt zusammen, um die genetische Architektur von Morbus Parkinson besser zu verstehen, und dies mit einem besonderen Fokus auf unterrepräsentierten Populationen. Das Ziel ist es, mindestens 150.000 neue Freiwillige zu untersuchen, darunter 50.000 nicht-europäische Personen aus Lateinamerika, der Karibik, Afrika, Indien, Südostasien und China sowie Minderheiten aus den USA.
Ich bin zuversichtlich, dass wir durch unsere globale Zusammenarbeit enorme Fortschritte zugunsten einer größeren Diversität bei genetischen Studien und bei der Minimierung von gesundheitlichen Ungleichheiten bei unterrepräsentierten Bevölkerungsgruppen machen werden. Ich möchte Sie ermutigen, sich diesen Bemühungen anzuschließen.
Danke an Emily Mason, ein neues Mitglied des Mata-Labors, für ihre Unterstützung beim Schreiben dieses Blog-Beitrags.





